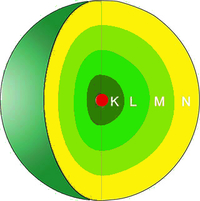
Atommodell nach Niels Bohr
In diesem Text erklären wir dir, welche Erkenntnisse Niels Bohr zu dem Atommodell lieferte und wie er das bestehende Modell weiterentwickelte. Dazu ist es wichtig die Grundlagen des Atommodells nach Ernest Rutherford zu kennen. Wenn dir dieses noch nicht geläufig ist, dann lies vorbereitend den Text zum Atommodell nach Rutherford.
- Über 700 Lerntexte & Videos
- Über 250.000 Übungen & Lösungen
- Gratis Nachhilfe-Probestunde
Wer war Niels Bohr?
Niels David Henrik Bohr war ein Physiker und Nobelpreisträger aus Dänemark, der von 1885 bis 1962 gelebt und geforscht hat. Er arbeitete zu seinen Lebzeiten mit einigen bedeutenden Forschern wie beispielsweise Heisenberg oder Rutherford zusammen. Zu seinen wichtigen Forschungsergebnissen gehört die Entwicklung eines Modells, das Aussagen über den Aufbau der Atome trifft. Dieses Modell basiert auf den Erkenntnissen von Ernest Rutherford, mit dem Bohr einige Zeit zusammengearbeitet hatte. Dieser hatte herausgefunden, dass Atome nicht, wie bis dahin angenommen, aus massiven "Kugeln" bestehen, sondern sich aus einem Atomkern und einer Atomhülle zusammensetzen. Der Kern besteht dabei aus positiv geladenen Protonen und neutral geladenen Neutronen. In der Hülle bewegen sich negativ geladene Elektronen um diesen Atomkern herum. Zwischen Kern und Hülle, so ergaben einige Versuche, die Rutherford durchführte, befindet sich nichts, also freier Raum.

Was besagt das Atommodell nach Niels Bohr?
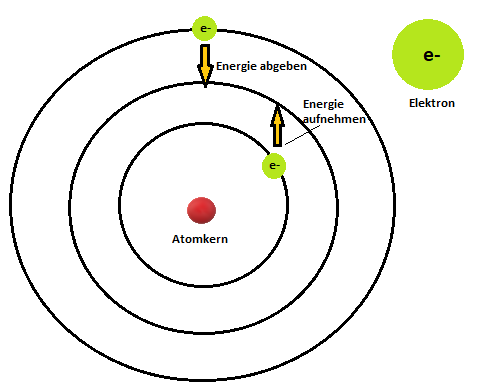
Niels Bohr griff die Erkenntnisse seines Kollegen auf und entwickelte dessen Theorie weiter. Er erkannte, dass die Elektronen nicht beliebig um den Kern kreisen, sondern dies in unterschiedlicher Nähe zum Kern tun. Die jeweiligen Abstände setzte er mit speziellen Energieniveaus gleich, die die Elektronen auf ihrer Kreisbahn um den Kern einnehmen. Vereinfacht kann man sagen, dass ein Elektron umso mehr Energie in sich gespeichert hat, desto weiter entfernt seine Flugbahn um den Kern eines Atoms verläuft. Da zu dem Abstand eines Elektrons jeweils ein bestimmtes Energieniveau gehört, gewinnt oder verliert ein Elektron Energie, wenn es von seiner Bahn abweicht, um auf eine andere zu gelangen. Die folgende Grafik veranschaulicht dir, wie das genau zu verstehen ist.
Merke
Je nach Abstand der Kreisbahn, auf dem sich ein Elektron um den Atomkern bewegt, hat dieses ein bestimmtes Energieniveau. Wenn ein Elektron von seinem Energiezustand zu einem anderen wechseln möchte, muss es entweder Energie abgeben ($\leftarrow$ näher zum Kern) oder Energie aufnehmen (weiter vom Kern entfernt $\rightarrow$).
Nun weißt du alles Wissenswerte über die Weiterentwicklung des Atommodells von Ernest Rutherford durch Niels Bohr und was man unter dem Begriff des Energieniveaus eines Elektrons versteht. Dieses Thema kannst du zudem noch mit dem Text Die Atomhülle und das Schalenmodell ergänzen. Dein neues Wissen kannst du jetzt an unseren Übungsaufgaben testen. Viel Spaß und Erfolg dabei!
Teste dein Wissen!
Mit wenigen Klicks die passenden Aufgaben und Lösungen zum Üben und Selbst-Lernen finden.
Hol dir Hilfe beim Studienkreis!
Selbst-Lernportal Online
Zugriff auf alle Aufgaben erhältst du in unserem Selbst-Lernportal. Bei Fragen helfen dir unsere Lehrer der online Hausaufgabenhilfe - sofort ohne Termin!
- Online-Chat 14-20 Uhr
- 700 Lerntexte & Videos
- Über 250.000 Übungsaufgaben
Einzelnachhilfe Online
Du benötigst Hilfe in Chemie? Dann vereinbare einen Termin bei einem Lehrer unserer Chemie-Nachhilfe Online. Lehrer zum Wunschtermin online fragen!
- Online-Nachhilfe
- Zum Wunschtermin
- Geprüfte Chemie-Nachhilfelehrer
Nachhilfe in deiner Nähe
Du möchtest Hilfe von einem Lehrer der Chemie-Nachhilfe aus deiner Stadt erhalten? Dann vereinbare einen Termin in einer Nachhilfeschule in deiner Nähe.
- Nachhilfe in deiner Nähe
- Zum Wunschtermin
- Geprüfte Chemie-Nachhilfelehrer
Unsere Kunden über den Studienkreis
Weitere Erklärungen & Übungen zum Thema